Contido
O óxidos básicos, tamén coñecido como óxidos metálicos, son os que combinan osíxeno cun elemento metálico. Dado que o osíxeno é altamente electronegativo e os metais son electropositivos, o enlace que se establece é iónico.
O fórmula elemental que representa todos os óxidos básicos é XO, onde X é o elemento metálico e O o osíxeno. Cada un destes pode ir seguido de subíndices (xeralmente 2 ou 3), que aparecen trocando as valencias (é dicir, a do metal coa do osíxeno).
Nomenclatura dos óxidos básicos
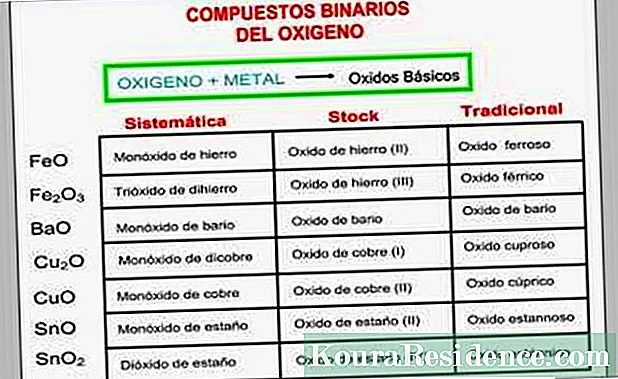
Nomenclatura tradicional: Os óxidos básicos noméanse mencionando primeiro o termo "óxido de" e despois o nome do elemento metálico ou "óxido" seguido dun adxectivo que é o nome do elemento metálico con diferentes terminacións, como se detalla a continuación:
- Nometais que só teñen un tipo de valencia (como sodio ou calcio), a parte do metal constrúese como unha palabra esdrújula coa terminación "ico".
- Nos metais que presentan dous tipos de valencia (como o cobre ou o mercurio), se o óxido ten a menor valencia, o nome do metal engádese co sufixo "oso" e é unha palabra seria. Se implica a maior valencia, o nome do metal engádese co sufixo "ico" e é unha palabra esdrújula.
- Cando hai tres valencias posibles (como o cromo), se o óxido ten a menor valencia, o nome do metal engádese co prefixo "hipo" e o sufixo "oso", e é unha palabra seria. Cando se trata da valencia intermedia, o metal chámase coa terminación "oso" e aínda é unha palabra grave, pero se implica a valencia máis alta, a terminación é "ico" e é unha palabra sdrújula.
- O metal que ten catro valencias posibles (como o manganeso), o esquema é o mesmo que o anterior para os tres primeiros, pero cando o metal se integra no óxido coa cuarta e maior valencia, o nome do metal engádese co prefixo "per" e o sufixo "ico", e é unha palabra esdrújula.
Nomenclatura deAccións: Baixo esta nomenclatura, os óxidos escríbense e denomínanse como "óxido de" + elemento metálico + número romano entre parénteses, o que indica a valencia coa que o elemento metálico está interactuando co osíxeno.
Nomenclatura sistemática: Actualmente é o preferido polo IUPAC(Unión Internacional de Química Pura e Aplicada), mantense o concepto de nomealos como "óxidos de", pero facéndoo precisamente engadindo o prefixo grego estándar que corresponde ao número de átomos de osíxeno (á palabra "óxido") e ao número de átomos metálicos (ao nome do metal) que contén cada molécula, empregando a preposición "de" como ponte.
Os óxidos básicos teñen innumerables usos na industria farmacéutica, pintura, materiais de construción, plásticos e outras industrias.
Exemplos de óxidos básicos
| trióxido de dialúmino | óxido manganoso |
| óxido de cobalto | óxido permangánico |
| óxido cúprico | óxido de calcio |
| óxido hipocrómico | óxido de cinc |
| óxido ferroso | óxido de cromo |
| óxido férrico | óxido crómico |
| óxido de magnesio | óxido mercúrico |
| ferruxe de plomo | trióxido de dimangano |
| óxido estannoso | trióxido de dicobalto |
| óxido estático | dióxido de titanio |
Outros tipos de óxidos:
- Óxidos metálicos
- Óxidos non metálicos
- Óxidos ácidos


